microRNA调控水牛朊病毒基因表达
赵卉
2017-7-11
朊病毒疾病,是一类由朊病毒蛋白引起的致死性神经退行性疾病。目前朊病毒疾病已在包括人在内的十多种动物中发现。其中,疯牛病因具有高度传染性和致死性而备受关注,因为它可通过食物链传染给人类。以往的研究表明PRNP基因是调控朊病毒疾病的关键基因,朊病毒蛋白表达量与朊病毒疾病的易感性呈正相关。
我们发现一个有趣的现象:全球有超过19万头的黄牛、瘤牛以及它们的杂交牛感染了疯牛病,但是却没有一例水牛被报道感染此病。我们的前期研究显示,在几个重要的组织中,水牛朊病毒蛋白的表达量显著低于黄牛,但是PRNP的表达受到了转录后的调控作用(Zhao et al, 2016, Science Bulletin)。为此,本研究我们从 microRNA调控入手,考察了其对基因的转录后调控作用。首先,我们对147个黄牛和146个水牛样本PRNP 3'UTR进行测序比对,结果共发现92个物种间差异固定位点。其中,对水牛PRNP 3'UTR出现的两个特异的插入位点和两个特异的突变位点(图1):28-bp的插入(g.970-997),AG的插入(g.1088-1089)和TG→CC的突变(1007-1008),进行miRNA结合预测,结果显示这些突变位点导致了15个miRNA特异地与水牛PRNP 3'UTR结合。荧光双报告实验证实,其中的miR-125b-5p, miR-132-3p, miR-145-5p, miR-331-3p和 miR-338-3p等5个miRNAs确实作用于这些物种间固定差异位点上(图2),进而特异性的调控水牛PRNP的表达。通过qPCR实验,我们进一步验证了这5个miRNAs和PRNP基因在水牛的脑闩组织中都存在共表达,而且miRNA的表达与朊病毒蛋白的表达呈负相关。以上研究结果揭示,这些miRNAs可通过作用于水牛PRNP 3'UTR特异突变区域,引起其mRNA的降解或者翻译抑制,从而特异地调控水牛PRNP转录后的表达从而使水牛PrP蛋白的表达量显著低于黄牛。本研究从miRNA转录后调控的角度,揭示了造成黄牛和水牛PrP蛋白表达差异的可能原因,也提示我们转录后表达调控的研究在朊病毒疾病研究中的重要性,这为朊病毒疾病易感性研究以及致病机制的解析提供了有意义的线索。相关工作以《Fixed differences in the 3'UTR of buffalo PRNP gene provide binding sites for miRNAs post-transcriptional regulation》为题2017年7月发表于Oncotarget杂志(2016IF=5.008)
http://www.impactjournals.com/oncotarget/index.php?journal=oncotarget&page=article&op=view&path[]=17545。
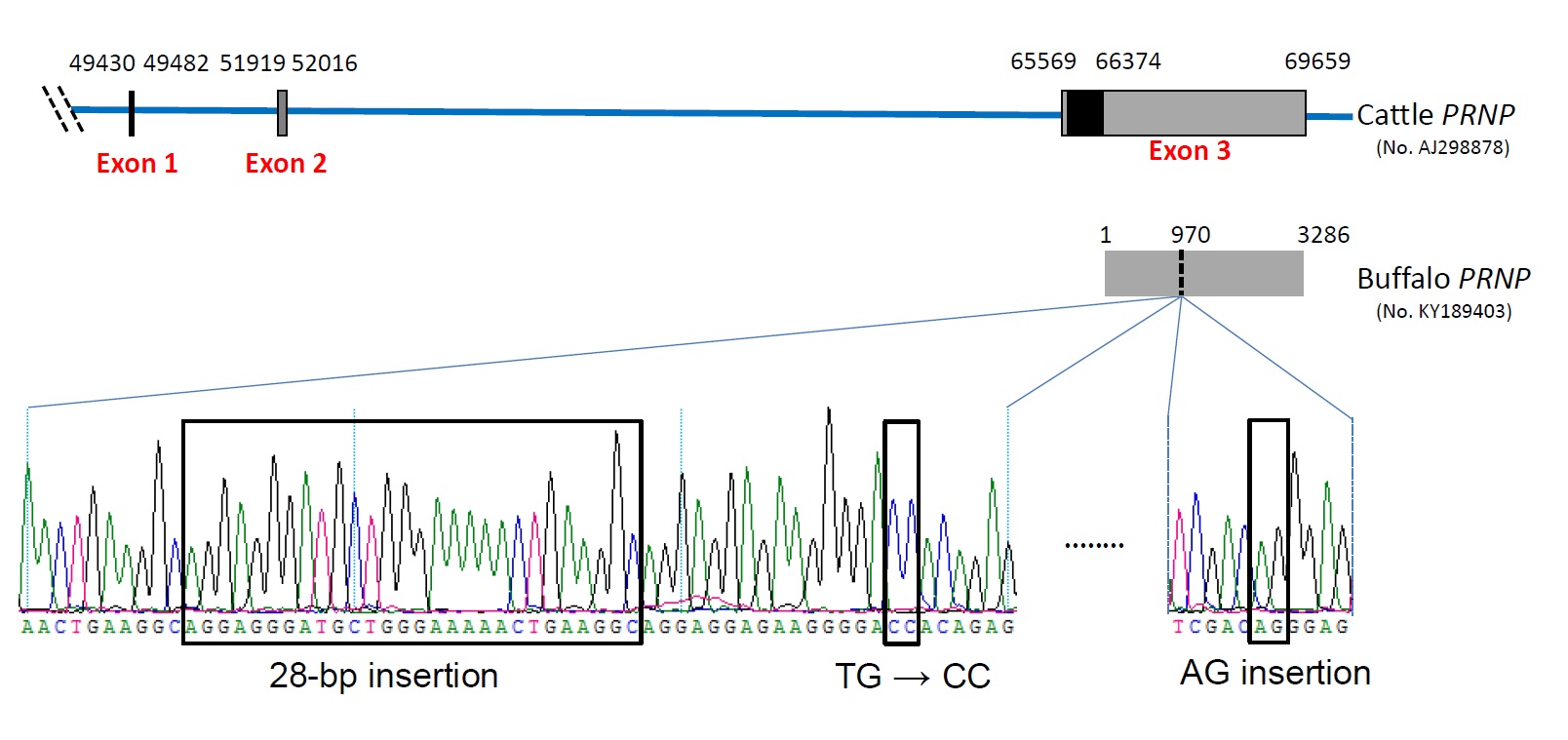
图1. 黄牛PRNP基因结构图示以及水牛PRNP基因3′UTR的四个显著差异位点。
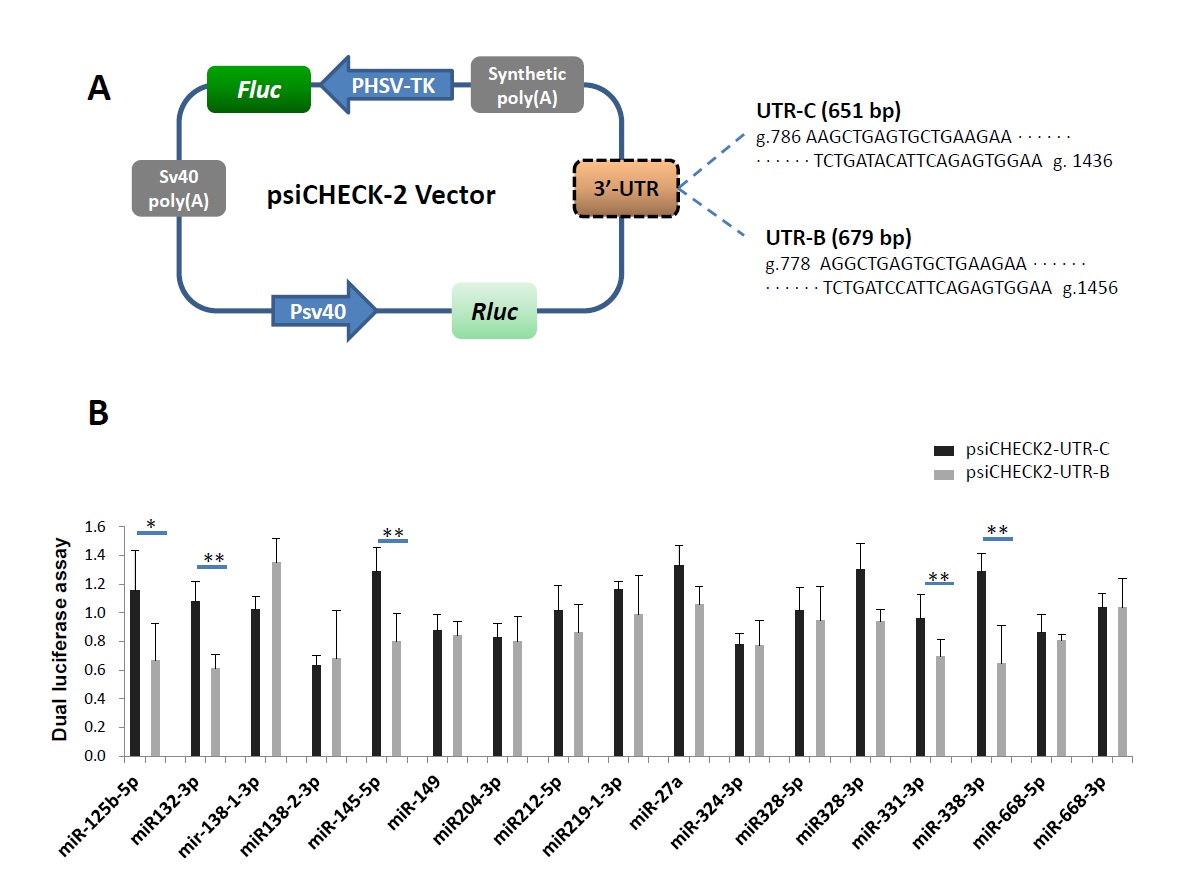
图2. 鉴定与黄牛PRNP基因3′UTR(UTR-C)或水牛3′UTR(UTR-B)相互作用的候选miRNA。